当前位置 : 网站首页 > 新闻中心 > 行业动态
近日,第一三共的EZHARMIA(Valemetostat,伐美妥司他)(DS-3201, DS-3201b)在日本获批上市,用于治疗难治性白血病、淋巴癌,成为第一款获得监管批准的EZH1/2 双重抑制剂。
伐美妥司他是一款first-in-class的EZH1/2双重抑制剂,在 T 细胞和 B 细胞淋巴瘤中都显示出活性,这使得它在治疗淋巴瘤的药物中脱颖而出,因为绝大多数药物只能治疗其中一种。临床实验显示伐美妥司他使 48% 的患者肿瘤缩小,包括 20% 治疗后没有癌症迹象的患者。
在中国,针对相同靶点的国产新药HH2835也正在中美同时进行临床试验。该药是海和生物与中国科学院上海药物所共同研究开发的一种新型、高效、特异 性的 EZH1/2 双重抑制剂,目前是国内唯一在中国申报临床研究的 EZH 抑制剂。
图1. 第一三共公司的Ezharmia(伐美妥司他 )获批用于治疗复发或难治性成人 T 细胞白血病/淋巴瘤
图源:fierce新闻
EZH1和EZH2都属于组蛋白甲基转移酶,是主要的表观遗传调控因子。表观遗传学药物,乍一听还比较陌生,但实际上相关研究已有50多年历史。
什么是表观遗传学?
表观遗传学(Epigenetics)是与遗传学(genetic)相对应的概念,表观遗传学被定义为“在基因组序列不变的情况下 ,可以决定基因表达与否并可稳定遗传下去的调控密码”。染色质凝聚、松弛结构的形成,以及开放、闭合等状态的转换提供了一种超越 DNA 序列本身的调控机制,即表观遗传调控。
肿瘤细胞通常利用表观遗传调控机制激活癌基因表达程序。与遗传变化不同,表观遗传变化是可逆的,不会改变我们的 DNA 序列,但它们可以改变我们身体读取 DNA 序列的方式。染色质是最早确定的癌症治疗靶点,早在20世纪70年代,科学家们就已经开始设计可以和DNA甲基化相关的改变染色质的促分化药物。
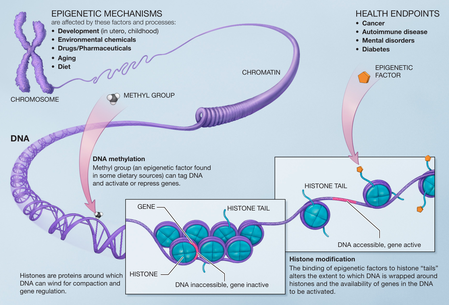
图2.表观遗传机制 图源:Wikipedia
而来自不同来源的化合物,包括中草药,食品和饮料,通过影响疾病发病过程中的表观基因组和基因表达的机制发挥有益的健康作用。通过针对所谓的表观遗传“读者”、“作者”和“擦除者”,化学物质可以逆转癌细胞和癌前阶段的异常表观基因组特征。因此,此类药物通过预防或治疗/治疗策略为癌症拦截提供了途径。之前大部分研究关注都集中在写入器(例如,组蛋白乙酰转移酶)和擦除器(例如,组蛋白脱乙酰酶)上,而较少关注表观遗传读取器(例如,组蛋白甲基转移酶)。
直到2012年哈佛大学科学家齐军合成的著名基因“开关分子” JQ1 被开发为表观遗传“读者”抑制剂,选择性地靶向BET家族成员 BRD4。将 JQ1 作为单药或与标准护理疗法联合进行的临床试验显示出抗肿瘤功效,但因为毒性或耐药性的问题需要进一步开发新一代靶向表观基因学相关靶点的药物。
表观遗传学药物开发策略
齐军博士最近在《药物化学杂志》特刊“表观遗传学 2022”发表综述,讨论了过去五年中针对表观遗传读取器,靶向组蛋白甲基转移酶(HMTs)的各种药物设计策略:包括非共价抑制剂、共价抑制剂、PROTACs降解剂等。
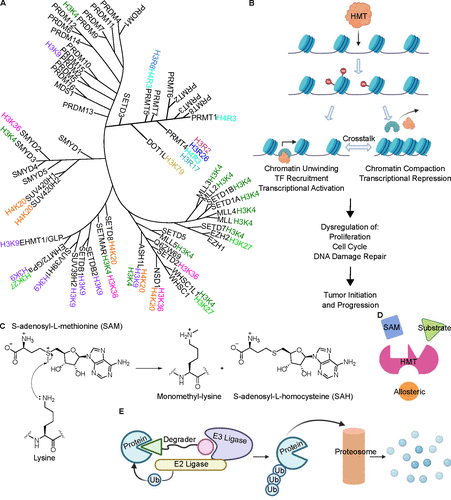
图3. 癌症中的组蛋白甲基转移酶及其靶向方法。(A) 人类组蛋白甲基转移酶的系统发育树,分为组蛋白赖氨酸甲基转移酶 (HKM) 和组蛋白精氨酸甲基转移酶 (HRM)。(B) 组蛋白甲基化失调可导致肿瘤发生和癌症进展。(C) 使用 SAM 辅因子的赖氨酸单甲基化机制。(D) 甲基转移酶抑制方法。(E) 通过 PROTAC 进行靶向蛋白质降解。
图源:齐军教授论文
组蛋白甲基转移酶(HMTs)的异常表达会导致癌症相关基因组蛋白甲基化异常,从而促进肿瘤发生。组蛋白甲基转移酶与化疗耐药和免疫刺激有关,使这些酶成为潜在的治疗靶点,小分子靶向这些蛋白质为癌症治疗中的新药开发提供了途径。
组蛋白甲基转移酶 (HMTs) 分为两类:赖氨酸甲基转移酶 (KMTs) 和精氨酸甲基转移酶 (PRMTs)。KMTs的失调与许多疾病的原因有关,包括癌症、精神健康障碍和发育障碍。KMTs可分为含 SET 结构域和非 SET 结构域。SET 结构域是组蛋白甲基转移酶的重要结构域,负责甲基转移酶的酶促活性,包括 SUV39, SET1, SET2, EZH (EZH1和EZH2已有药物上市),RIZ (PRDM, SMYD, SUV420) 等家族。而不含 SET 结构域的蛋白较少,如 DOT1L 蛋白。DOT1L 是已知的靶向组蛋白 H3K79 位置的组蛋白甲基转移酶。在过去的十年中,在开发靶向参与组蛋白甲基化和表观遗传调控的 KMT 的药物方面取得了重大进展。这些抑制剂中的第一个里程碑泰泽思他(tazemetostat),2020年被批准用于治疗上皮样肉瘤和滤泡性淋巴瘤,目前该药国内的三期临床也在进行中。
而PRMTs 目前在哺乳动物中鉴定出九种,根据其催化活性可分为三类,催化精氨酸的单甲基化 (MMA),不对称 (ADMA) 或对称二甲基化 (SDMA)。I 型 PRMTs (PRMT1, PRMT2, PRMT3, PRMT4, PRMT6 和 PRMT8) 产生单或不对称二甲基化精氨酸 (ADMA),II 型 PRMTs (PRMT5 和 PRMT9) 产生单或对称二甲基化精氨酸 (SDMA)。而 Ⅲ 型的 PRMT7,只产生 MMA。由于 PRMT 家族成员在各种癌症类型中的作用越来越重要,因此新药研发管线有很多针对 PRMT 家族成员的选择性抑制剂。PRMT4、PRMT5 和 PRMT7 已成为越来越有希望的治疗靶点,因为有报道称这些蛋白质的过表达和失调促进了一系列实体癌和血癌的肿瘤发生。这些酶不仅可以作为单一疗法的靶点,也可以用于克服耐药性和促进免疫反应的组合策略。
针对 EZH2、DOT1L 和多个 PRMT 家族成员的多种抑制剂已经开发成功或正在进行临床实验。比如Epizyme旗下的DOT1L抑制剂pinometostat(EPZ-5676)进入了临床试验,但其临床活性不高。G9A抑制剂EZM8266、PRMT5抑制剂等。
国内上海科技大学也报道过非核苷类DOT1L抑制剂DC_L11。为了克服抑制剂的不足最近文献报道了不少靶向HMT的 PROTAC降解剂:例如通过将 CRBN结合子沙利度胺与模仿 SAM结构的 EZH2 抑制剂 GSK126 和 EPZ6438(Tazemetostat)相结合,开发了一系列 EZH2 特异性 PROTAC。与 EZH2 抑制剂相比,基于 GSK126 的降解剂对 EED 和 SUZ12 的降解能力更强,此外,EZH2 的完全降解被证明可以消除其致癌功能,包括减少甲基化,这是目前 EZH2 抑制剂没有实现的壮举。
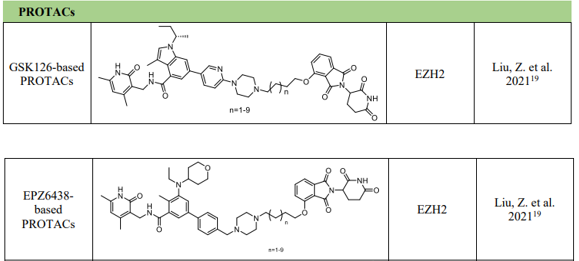
图4 靶向EZH2的降解剂结构。图源:参考文献
靶向组蛋白甲基化修饰的蛋白抑制剂一览
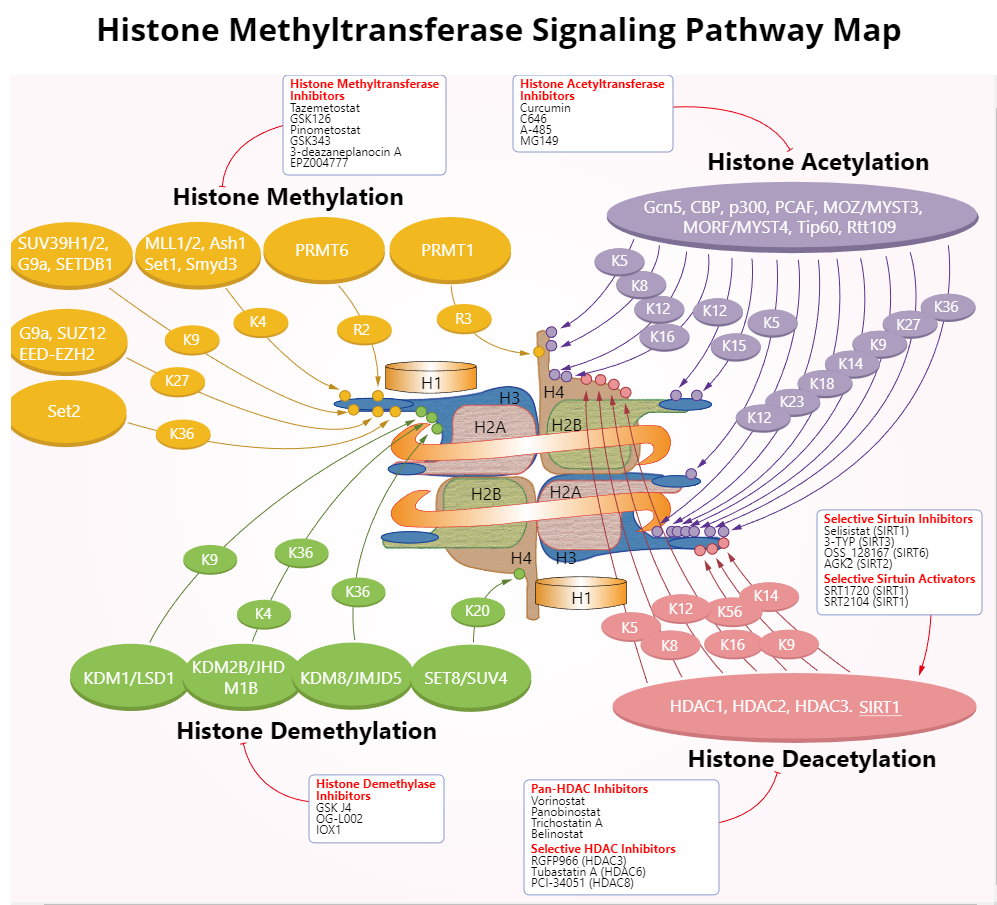
图 5 组蛋白甲基转移酶信号通路图
图源:Selleck
小 结
靶向 HMT 的小分子抑制剂和降解剂已显示出用于癌症治疗的巨大潜力,这从进入临床试验开发阶段的抑制剂数量、化学生物学方法的持续进步以及对 HMT 在疾病中作用的科学兴趣的增加可以看出状态和作为药物反应的介质将导致这些化合物的进一步开发和改进。
与此同时,高通量化合物筛选平台的进步和可用性的增加大大扩展了已经存在的潜在 HMT 选择性抑制剂的范围。此外,计算化学方法,包括使用晶体结构和分子对接也使得新药研发有了更多工具。
尽管 HMT 靶向化合物开发取得了令人兴奋的进展,但与激酶抑制剂和传统化疗相比,表观遗传修饰探针作为一个整体在化合物有效性所需的时间方面仍存在不足。另一方面表观遗传治疗进展还是主要集中在血液肿瘤,实体瘤还需要更多的工作。
表观遗传学诞生已经接近50年,相关研究越来越深入;尽管已经填补了一些知识空白,而更多的疑问也不断涌现。另一个挑战是大多数表观基因改变为功能丢失性突变,很难治疗。表观遗传药物和经典化疗、靶向药物、其他表观遗传药物以及免疫检查点抑制剂联合使用也许比单药使用效果更好。
总之,表观遗传相关的蛋白是一类重要的治疗靶点。考虑到潜在靶点数目之多,需要系统发现和验证潜在药物靶点来进行药物研发,才能达到理想疗效。
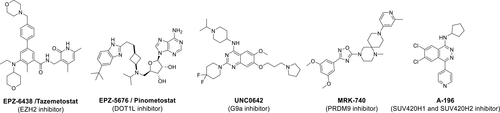
图6一些选择性抑制剂的结构
图源:参考文献
参考文献:
1. 表观遗传学
https://www.encyclopedie-environnement.org/zh/sante-zh/epigenetics-how-the-environment-influences-our-genes/
2. 齐军教授综述
https://pubs.acs.org/doi/pdf/10.1021/acschembio.2c00062
3. 表观遗传2022特刊
https://pubs.acs.org/page/vi/epigenetics
4. JQ1的故事
https://open.163.com/newview/movie/free?mid=MA47G39CR&pid=MA44S7L2U
来源:药智头条